Theo Cục Quản lý dược, báo cáo của các đơn vị nhập khẩu cho thấy khả năng cung ứng vắc xin phòng dại trong năm 2018 là đủ để cung ứng cho nhu cầu tiêm chủng.

tin liên quan
Bộ Y tế khuyến cáo tiết kiệm vắc xin phòng dạiNhư vậy, khả năng cung ứng vắc xin phòng dại trong năm 2018 cho thị trường VN chỉ tính riêng Verorab, Abhayrab và Indirab (chưa bao gồm Speeda) là 2,193 triệu liều (cao gấp 149% so với tổng số lượng vắc xin phòng dại đã nhập khẩu trong năm 2017 và cao gấp 169% so với số lượng vắc xin phòng dại sử dụng trung bình mỗi năm).
Theo đánh giá của Cục Quản lý dược, đặc thù của vắc xin phòng dại là nhu cầu sử dụng phụ thuộc vào số lượng người dân bị súc vật cắn. Vì vậy, việc tiên lượng, dự báo nhu cầu vắc xin phòng dại là tương đối khó khăn hơn so với các loại vắc xin khác. Trong khi đó, hợp đồng ký giữa các cơ sở cung ứng vắc xin với các đơn vị tiêm chủng đa phần là hợp đồng nguyên tắc, không có số lượng cụ thể nên khó khăn cho các cơ sở cung ứng trong việc cung cấp vắc xin, nhất là khi nhu cầu tăng.
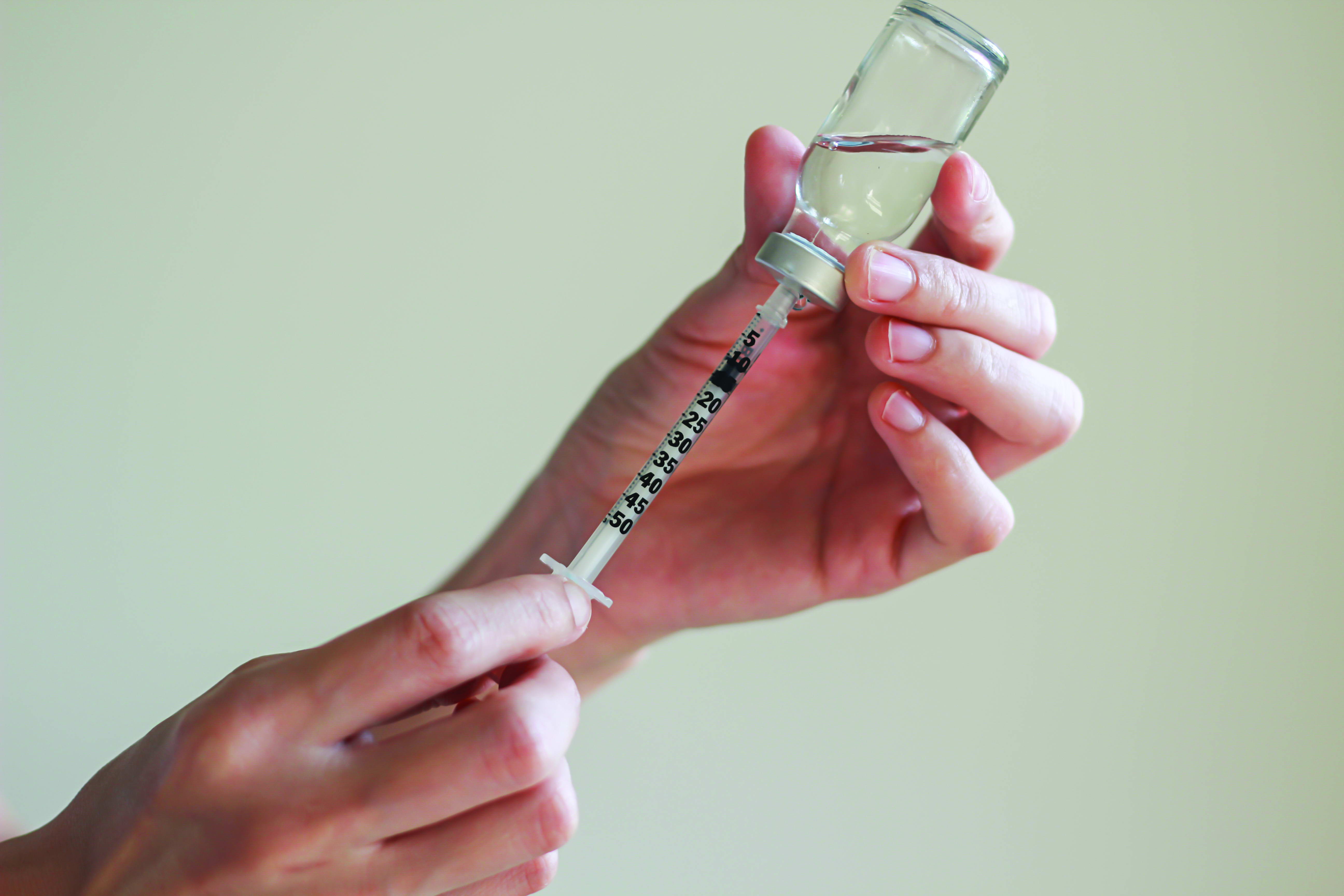
Việc tiên lượng, dự báo nhu cầu vắc xin phòng dại là tương đối khó khăn hơn so với các loại vắc xin khác
|
Ưu tiên thẩm định nhanh
Theo ông Đỗ Văn Đông, Phó cục trưởng Cục Quản lý dược, ngay từ đầu năm nay 2018, Cục đã có công văn gửi các cơ sở sản xuất, đăng ký, nhập khẩu vắc xin (bao gồm cả vắc xin phòng dại), đề nghị các cơ sở báo cáo kế hoạch sản xuất, cung ứng vắc xin và báo cáo các trường hợp dự kiến có giảm nguồn cung, khoảng thời gian dự kiến sẽ giảm và kế hoạch khắc phục.
“Chúng tôi đã chủ động ưu tiên thẩm định nhanh các hồ sơ đăng ký đề nghị thay đổi bổ sung đối với các vắc xin phòng dại hiện đang trong quá trình lưu hành tại VN (vắc xin Speeda, vắc xin Indirab). Riêng đối với vắc xin Speeda, khi công ty phân phối nhập khẩu về 2.200 liều vắc xin Speeda nhưng do cơ sở chưa nộp hồ sơ thay đổi bổ sung nên Viện Kiểm định vắc xin quốc gia chưa thể cho xuất xưởng. Ngay sau khi nhận được hồ sơ bổ sung ngày 12.4.2018 của công ty nhập khẩu liên quan đến vắc xin Speeda, ngày 24.4.2018 Cục đã có công văn chấp thuận hồ sơ thay đổi bổ sung của công ty. Vì vậy, hiện 2.200 liều Speeda đã có thể xuất xưởng và đưa ra cung ứng cho các cơ sở tiêm chủng.
Để an toàn cho người bệnh và sử dụng vắc xin đúng chỉ định, Cục Quản lý dược cũng đề nghị các cơ sở tiêm chủng vắc xin chủ động dự trù, đặt hàng, ký hợp đồng cụ thể, kịp thời theo từng vắc xin đối với từng đơn vị cung ứng để tránh rủi ro khi một vắc xin bị thiếu hụt thì có vắc xin khác thay thế.
|
Mất 6 - 12 tháng để sản xuất
Vắc xin phòng dại được sản xuất bằng công nghệ sinh học với nhiều công đoạn phức tạp (tạo ngân hàng chủng vi rút từ vi rút gốc, tạo chủng làm việc...), thời gian cần thiết trung bình cho sản xuất là từ 6 - 12 tháng; từng lô sản xuất/nhập khẩu phải được kiểm định trong nước và nước ngoài, và chỉ được lưu hành sau khi có kết quả kiểm định đạt yêu cầu. Ngoài ra, do yêu cầu cao về công nghệ nên số lượng nhà sản xuất trên toàn thế giới ít.
(Theo Cục Quản lý dược, Bộ Y tế)
|



Bình luận (0)